Молочная кислота
Группа веществ:
Органические кислоты
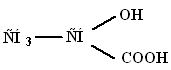
Молекулярная масса 90,1; бесцветные кристаллы. Известны D(+)-молочная кислота, D(–)-молочная (мясо-молочная) кислота и рацемическая молочная кислота – молочная кислота брожения. Для D,L- и D-молочных кислот – t плавления соответственно 18 °С и 53 °С; t кипения соответственно 85 °С/1 мм рт.ст. и 103 °С/2мм рт.ст.; для D-молочной кислоты удельное оптическое вращение для D-линии натрия при температуре 20˚С: [α]D20 -2,26 (концентрация 1,24% в воде). Для D,L-молочной кислоты ∆H0образования - 682,45 кДж/моль; ∆H0плавления 11,35 кДж/моль; ∆H0испарения 110,95 кДж/моль (25°С), 65,73 кДж/моль (150°С). Для L-молочной кислоты ∆H0сгорания - 1344,8 кДж/моль; ∆H0обpазования -694,54 кДж/моль; ∆H0плавления 16,87 кДж/моль.
Из-за высокой гигроскопичности молочной кислоты обычно используют ее концентрированные водные растворы – сиропообразные бесцветные жидкости без запаха. Для водных растворов молочной кислоты плотность г/см3 при температуре 20˚С d420 1,0959 (40%), 1,1883 (80%), 1,2246 (100%); удельное оптическое вращение для D-линии натрия при температуре 25˚С: [α]D25 1,3718 (37,3%), 1,4244 (88,6%); h 3,09 и 28,5 мПа∙с (при 25 ˚С) соответственно для 45,48 и 85,32%-ных растворов; g 46,0.10-3 Н/м (25°С) для 1 М раствора; е 22 (17°С). Молочная кислота растворяется в воде, этаноле, плохо – в бензоле, хлороформе и др. галогенуглеводородах; рKа 3,862 (при 25°С); рН водных растворов 1,23 (37,3%), 0,2 (84,0%).
Окисление молочной кислоты обычно сопровождается разложением. При действии HNO3 или О2 воздуха в присутствии Сu или Fe образуются НСООН, СН3СООН, (СООН)2, СН3СНО, СО2 и пировиноградная кислота. Восстановление молочной кислоты HI приводит к пропионовой кислоте, а восстановление в присутствии Re-черни – к пропиленгликолю.
Молочная кислота дегидратируется до акриловой кислоты, при нагревании с НВr образует 2-бромпропионовую кислоту, при взаимодействии Са-соли с РСl5 или SОСl2-2-хлорпропионилхлорид. В присутствии минеральных кислот происходит самоэтерификация молочной кислоты с образованием лактона, а также линейных полиэфиров. При взаимодействии молочной кислоты со спиртами образуются гидроксикислоты RCH2CH(OH)COOH, а при взаимодействии солей молочной кислоты со спиртамиэфиры. Соли и эфиры молочной кислоты называются лактатами.
Молочная кислота образуется в результате молочнокислого брожения (при скисании молока, квашении капусты, солении овощей, созревании сыра, силосовании кормов); D-молочная кислота обнаружена в тканях животных, растений, а также в микроорганизмах.
В промышленности молочную кислоту получают гидролизом 2-хлорпропионовой кислоты и ее солей (100 °С) или лактонитрила CH3CH(OH)CN (100°С, H2SO4) с последующим образованием эфиров, выделение и гидролиз которых приводит к продукту высокого качества. Известны другие способы получения молочной кислоты: окисление пропилена оксидами азота (15-20°С) с последующей обработкой H2SO4, взаимодействием СН3СНО с СО (200 °С, 20 МПа).
Молочную кислоту применяют в пищевой промышленности, в протравном крашении, в кожевенном производстве, в бродильных цехах в качестве бактерицидного средства, для получения лекарственных средств, пластификаторов. Этил- и бутил-лактаты применяют в качестве растворителей эфиров целлюлозы, олиф, растительных масел; бутил-лактат – также как растворитель некоторых синтетических полимеров.
Хроматограммы образцов, содержащих это вещество
| Название | Колонка | Детектор |
|---|---|---|
| Стандартная смесь органических кислот | Rezex ROA-Organic Acid 300х7.8 мм 8 мкм | Спектрофотометрический |
| Органические кислоты в браге | Rezex ROA-Organic Acid 300х7.8 мм 8 мкм | Спектрофотометрический |
| Органические кислоты в соке виноградном | Rezex ROA-Organic Acid 300х7.8 мм 8 мкм | Спектрофотометрический |
| Углеводы, спирты, органические кислоты в браге | Rezex ROA-Organic Acid 300х7.8 мм 8 мкм | Рефрактометрический |
| Стандартная смесь углеводов, спиртов, органических кислот | Rezex ROA-Organic Acid 300х7.8 мм 8 мкм | Рефрактометрический |
