Цистин
Группа веществ:
Аминокислоты
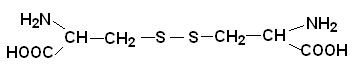
Молекулярная масса 240,24. L-Цистин - бесцветные кристаллы; удельное оптическое вращение для D-линии натрия при температуре 20°С: [α]D20 -223,4° (1 г в 100 мл 1 н. НСl); растворим в воде; при 35°C рКа 1,0 и 2,1 (СООН), 8,02 и 8,71 (NH2). Для D-Цистина удельное оптическое вращение для D-линии натрия при температуре 20°С: [α]D20+223° (1 г в 100 мл 1 н. НСl). Образуется при окислении цистеина кислородом воздуха в щелочных растворах. Синтез пептидов, содержащих цистин, осуществляют окислением групп SH цистеина.
L-Цистин - заменимая некодируемая α-аминокислота, не включается в пептидную цепь при ее биосинтезе, а образуется в результате ферментативного окисления остатков двух молекул цистеина (в т. ч. из разных полипептидных цепей).
Цистин играет важную роль в формировании пространственных структур ряда белков и пептидов, например инсулина, соматостатина и иммуноглобулинов. Данные спектра ПМР у цистина такие же, как у цистеина. Цистин впервые выделен К. Мёрнером в 1899 г. из рога.
Хроматограммы образцов, содержащих это вещество
| Название | Колонка | Детектор |
|---|---|---|
| Стандартная смесь аминокислот 1 | Synergi Fusion-RP 250х4.6 мм 4 мкм | Спектрофотометрический |
| Стандартная смесь аминокислот 2 | Synergi Fusion-RP 250х4.6 мм 4 мкм | Спектрофотометрический |
